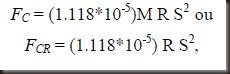Início » Posts etiquetados como 'Física Aplicada'
Arquivo da tag: Física Aplicada
Tutorial: Como usar o Espectrofotômetro e como criar uma curva de calibração Abs no Excel
Assista a uma aula prática de química experimental. Tema: Usando o espectrofotômetro
.::Espectrofotometria de absorção no UV-Visivel (ou Análise colorimétrica por espectrofotômetro)::.
A espectrofotometria pode ser definida como toda técnica analítica que usa a luz para medir as concentrações das soluções, através da interação da luz com a matéria.
.::Fundamentos::.
A luz de uma maneira geral é mais bem descrita como uma radiação eletromagnética em virtude de sua natureza dualística. Ou seja, ela existe e tem um comportamento de campos elétricos e magnéticos oscilantes como a figura abaixo representa:
Onde:
O comprimento de onda (λ) é a distância em metros, de um pico ao outro da onda.
A frequência (v) é o grau de oscilação das ondas em função da velocidade da luz no vácuo, que é representada pela constante c (c=2,998×108m.s-1). De modo que:
λ . v = c
.::Espectro eletromagnético representando os comprimentos de onda correspondente a cada radiação::.
A técnica espectroscópica é baseada no aumento de energia em função do aumento da frequência da radiação incidida. Quando uma espécie química absorve energia na forma de fótons, seus elétrons ficam excitados e ocorre uma transição de um orbital de mais baixa energia para outro de maior energia.
O aumento de energia é representado pela condição de frequência de Bohr:
E = hv
Onde:
E : é a energia que aumenta em função da frequência, e
h: é a constante de Planck h=6,626×10-34J.s.
A espectrofotometria consiste em usar o espectro radiante para estudar as soluções biológicas e químicas. No procedimento básico, um feixe de energia atravessa a solução, e sua absorção oferece informações sobre a qualidade e quantidade dos componentes presentes. Para as análises espectrofotométricas, a faixa do espectro de radiação mais utilizada vai do ultravioleta (λ = 200 nm) até o infravermelho (λ = 1000 nm). A faixa do visível vai de 400 a 750 nm, onde os seres humanos experimentam uma gama de sensações visuais denominada cores.
A luz usada em espectrofotometria é chamada luz monocromática, pois é referente a um único comprimento de onda que é obtido através de um espectrofotômetro:
Figura 1: Esquema do Espectrofotômetro: A fonte de luz tem seu feixe focalizado pelo colimador (C) sobre um prisma de quartzo. A luz é decomposta em ultravioleta (UV), violeta (VI), azul (AZ), verde (VE), amarelo (AM), laranja (LA), vermelho (VR) e infravermelho (IV). Ume fenda seletora escolhe uma fina porção desse espectro como luz monocromática (luz MC). A luz MC passa através da cubeta que contém a solução, e parte é absorvida, parte transmitida. Uma fotocélula acoplada a um galvanômetro mede a luz transmitida. A diferença é a luz absorvida. O galvanômetro tem uma escala especial de 0,0 a 2,00, que indica leituras lineares (aritmeticamente proporcionais à absorção da luz). As fontes de luz para ultravioleta são geralmente lâmpadas de Hidrogênio, ou de Deutério. Para o visível e infravermelho, lâmpadas de tungstênio e irradiadores de cerâmica são usados. A decomposição da luz é feita, além de primas, por grades de difração. Um método simples de obter luz MC é usar filtros, que são pedaços de vidro colorido especiais, que deixam passar a luz da sua cor. A luz MC dos filtros é de qualidade inferior à dos primas e grades.
É possível obter comprimentos de onda que sejam específicos para certas substâncias através da construção de uma curva de absorção espectral (varredura); onde a substância em questão (aquela que se quer determinar) é colocada na cubeta, e os comprimentos de onda do UV até o IV vão sendo passados, e a absorção de cada faixa é medida. O comprimento de onda a ser ajustado no aparelho será aquele onde tiver ocorrido a maior absorbância, pois, em essência se trata do pico de absorção de energia pela molécula. Ex: Para a análise do teor de glicose deve-se ajustar o aparelho em 500 nm, pois, se trata da maior absorbância para esta molécula.
Como as moléculas de substâncias diferentes têm níveis moleculares de energia diferentes, ocorre que cada substância absorve a radiação de maneira peculiar. Uma vez conhecido o espectro de absorção de uma substância pode-se determinar também em que quantidade essa substância se apresenta em uma solução analisada. Isso é feito através da medida da intensidade de luz que atravessa a amostra.
Quando a luz incide sobre uma substância pode ocorrer reflexão, refração, espalhamento ou absorção pelo material.
O processo de absorção ocorre a nível molecular. A absorção da radiação se dá quando a energia que ela transporta é igual a diferença entre dois níveis de energia da molécula.

A = log Po/P = log 1/T = – log T
Ex: Ausência de absorção à P = Po à T = 1 à A = 0
90% de luz absorvida à 10% transmitida à P = Po/10 à A = 1
A = ε . b . c
A = absorbância (adimensional)
b = caminho ótico (cm)
c = concentração (mol. L -1)
ε = absortividade molar (mol-1 . L . cm -1) à característico de cada substância em cada λ
A lei de Lambert & Beer
A força vital da espectrofotometria está fundamentada na lei de Lambert-Beer, que estabelece:
“A absorbância é diretamente proporcional a concentração da solução de amostra.”
Ou:
Log(I/I0) = εcl
A = εcl
Onde:
A: é a absorbância,
ε: é o coeficiente de extinção molar
I: é o comprimento da cubeta
É possível, por simples comparação visual, determinar a concentração aproximada de uma solução colorida comparando-a com soluções do mesmo soluto que tenham concentrações conhecidas. Quando dispomos de aparelhos capazes de medir a intensidade da luz transmitida pelas soluções (fotocolorímetros ou espectrofotômetros) podemos determinar a concentração da solução desconhecida pela aplicação da lei de Lambert & Beer que correlaciona a intensidade da luz transmitida com a concentração do soluto na amostra.
Lei de Lambert – Quando a concentração da substância é constante, a absorção depende do comprimento do trajeto óptico.
Lei de Beer – Quando o trajeto óptico é constante, a absorção depende da concentração.
Combinando as duas leis, Absorção é proporcional ao trajeto óptico e à concentração.
Abs = a.c.l
O que demonstra que a Absorbância (Abs) de uma solução é proporcional (relação linear) à concentração do soluto corado (c).
A partir da proporcionalidade entre absorbância e concentração é possível obter uma curva de calibração, ou seja, um gráfico relacionando a Abs e a Concentração da amostra.
Figura: Curva de Calibração para Método Enzimático (GOD-POD) de detecção de glicose.
R2 é chamado de coeficiente de determinação e junto ao coeficiente de correlação R é um indicativo da linearidade do método desenvolvido. Métodos devem ter linearidade alta, ou seja, próximas a 1,0000 para que possam ser utilizados em uma técnica espectrofotométrica.
A equação da reta y=a.x + b permite a relação direta entre a absorbância (y) e a concentração presente na amostra (x). Assim:
Abs = a.[concentração] + b
Para o exemplo acima temos:
Abs = 0,3496.[glicose] – 0,0011
A partir da equação de reta é possível determinar o valor de concentração para qualquer amostra analisada no espectrofotômetro. Exemplo:
Amostra resultou em Abs = 0,356.
Pela equação: 0,356=0,3496x[glicose]-0,0011
0,356+0,0011 = 0,3496x[glicose] (troca de lado, mudando o sinal, para isolar [glicose])
0,3571 = 0,3496 x [glicose]
0,3571/0,3496 = [glicose] (passa dividindo para isolar [glicose])
1,021 mg/mL = [glicose]
.::Passo a Passo para a análise espectrofotométrica::.
- Ligar o espectrofotômetro e esperar 30 min para aquecimento e estabilização dos circuitos.
- Ajustar o comprimento de onda (nm).
- Colocar a estrutura escura (cubeta). Feche a tampa e aperte 0%T (zerar selecionando o T). Escolher o T entre os indicadores A e T. Com isso você calibrou o 0% da Transmitância.
- Preencha uma das cubetas com água destilada ou o solvente usado puro.
- Colocar a cubeta com o branco no compartimento de amostras.
- Ajustar o branco apertando 0A/100%T. Ou dependendo do modelo, apenas zerar selecionando o A.
- A amostra deve ser preparada com a quebra da mesma por métodos mecânicos, químicos ou físicos.
- A amostra é solubilizada no solvente escolhido em um balão volumétrico limpo e seco. IMPORTANTE: o solvente na maioria das vezes é água destilada, porém, quando tratar-se de amostras apolares que precisam ser diluídas em solventes orgânicos NUNCA utilize alcenos, alcinos, cetonas ou qualquer outro que tenha ligações C=C ou C=O ou ligações triplas!!!
- A amostra deve ser filtrada em uma membrana de 0,2 µm, por que a solução deve estar totalmente límpida a fim de diminuir ao máximo o erro causado por partículas em suspensão. A cubeta contendo o branco é retirada do equipamento e sua absorção anotada. Após esse processo a solução de interesse é lida, e dessa absorbância é subtraído a leitura do branco.
.::IMPORTANTE::.
- É imprescindível que o equipamento seja calibrado e manuseado de acordo com as instruções do fabricante, que especifica a margem de erro que o aparelho tem.
- Para evitar erros de leitura sempre certificar-se de que o equipamento esteja fechado. Antes da leitura, a luz do ambiente pode interferir no resultado.
- Manter o equipamento sempre limpo e fechado a fim de evitar o acúmulo de partículas de poeira que interferem na análise. Em hipótese alguma toque a cubeta com as mãos sem luvas, pois nossas mãos contêm gordura que interfere na leitura.
- Somente podem ser analisados por espectrofotometria de absorção compostos que absorvem luz.
- Em caso de soluções fortemente coloridas, como permanganatos, complexos altamente coloridos, dicromatos, cromatos e outros compostos com cores altamente acentuadas deverão ser feitas no mínimo 5 diluições de concentração conhecida e lidas no espectrofotômetro e uma curva analítica deverá ser traçada afim de determinar o coeficiente de extinção molar. Soluções muito concentradas tendem a provocar erros de leitura porque existem muitas moléculas próximas umas das outras.
.::Como criar uma curva de calibração ABS no Excel::.
- Abra o Excel e escolha uma planilha em branco.
- Usando os dados coletados nas leituras no espectrofotômetro crie uma tabela com os valores de concentração à esquerda e ABS (absorbância) à direita como no exemplo abaixo:
- Clique na aba inserir
- Selecione na tabela somente os valores como na figura abaixo:
- Selecione nos tipos de gráficos Dispersão:

- Em Dispersão selecionar a opção com linhas suaves e marcadores – Comparar pares de valores que representam uma função. Também pode ser encontrado como Dispersão – f(x).

- O gráfico será montado automaticamente. Após isso vá em Layout do gráfico e clique nas setas até encontrar um modelo fx. Clique nele.
- O resultado será esse. Aparecerá a equação da reta.
Espero ter ajudado!
Fontes:
- Apostila de Espectrofotômetro – Prof. Luis Carlos Neves
- Prática Laboratorial dirigida pelo Prof. Luis Carlos Neves
Física Aplicada – Centrifugação
Disciplina – Física Aplicada
Prof. Luiz Carlos M. Neves
Assunto: Centrifugação
1. Introdução.
A centrifugação é uma operação unitária amplamente utilizada nas áreas industriais e em bioquímica, biotecnologia, biologia celular, molecular, com a principal finalidade de separação de frações ou a concentração das moléculas de interesse. Pode ser realizada com o objetivo de separar sólidos de líquidos ou mesmo uma mistura de líquidos.
Uma partícula em movimento linear continuará em velocidade constante e uniforme se não for influenciada por forças externas.
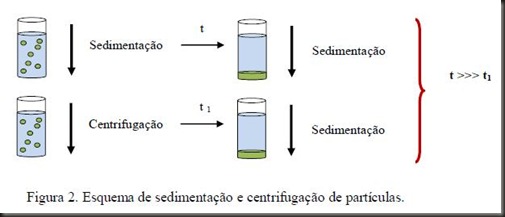
Quando uma partícula é submetida a uma força centrífuga (g) para isolar partículas suspensas em seu meio, seja da forma em lotes ou fluxo contínuo, esta sedimentação é forçada. As aplicações de centrifugação são muitas e incluem testes de análises clínicas, testes bioquímicos, a sedimentação de células e vírus, a separação de massa celular, isolamento de DNA, RNA, proteínas ou lipídios ou até mesmo para secar a roupa ou a salada em casa (Figura 1).
2. Aumento no efeito da gravidade: a centrífuga.
Se uma suspensão for deixada em repouso, as partículas dispersas irão se assentar por meio do fenômeno de decantação ou sedimentação, por ação da gravidade (g = 9,8 cm/s2). Primeiro serão sedimentadas as partículas maiores e depois as menores em valores de tempo variáveis, o que dificulta determinar o término da operação. Através da centrifugação este tempo é acelerado, pois pequenas partículas podem ser separadas com a aplicação da força centrífuga. Se compararmos com a filtração, a centrifugação é mais cara, porém a principal desvantagem da filtração é a possibilidade rápida de entupimento dos filtros, dependendo do tipo de material utilizado.
Quando uma suspensão de partículas é centrifugada a sedimentação das partículas é proporcional à força aplicada. As propriedades da solução também irão interferir na taxa de sedimentação.
3. O que é a força centrífuga?
Qualquer corpo ou partícula que apresente um movimento circular uniforme está submetido a uma força centrífuga, que tem como referência, o centro da trajetória circular que a partícula descreve, e pode ser representada pela relação:
![]() onde:
onde:
m = massa do corpo;
ω = velocidade angular do movimento de rotação e,
r = raio de rotação
Quanto maior for o número de rotações por segundo, maior será a força centrífuga aplicada na partícula e, quanto maior o raio da circunferência, maior a força centrífuga. A força centrífuga relativa (FCR) pode ser calculada por:
Onde:
R = raio de centrifugação, em m ou cm,
N = velocidade de centrifugação em rotações por minuto (rpm).
Quando uma suspensão é submetida a uma velocidade ou a um número de revoluções por minuto (RPM), a força centrífuga faz com que as partículas se afastem radialmente do eixo da rotação. A força aplicada nas partículas é chamada de Força Centrífuga Relativa (RCF). Por exemplo, um RCF de 500g indica que a força centrífuga aplicada é 500 vezes maior que a força gravitacional da Terra.
Quando se pretende separar componentes biológicos ou realizar a purificação de proteínas de interesse industrial, a operação unitária de centrifugação é bastante utilizada, podendo ser combinada com outras técnicas, dependendo da necessidade do produto. A centrifugação separa partículas por diferencial de tamanho ou densidade, enquanto que a eletroforese separa as partículas baseadas na carga elétrica; a cromatografia por solubilidade, dimensão, carga elétrica e a partição pela solubilidade do produto de interesse.
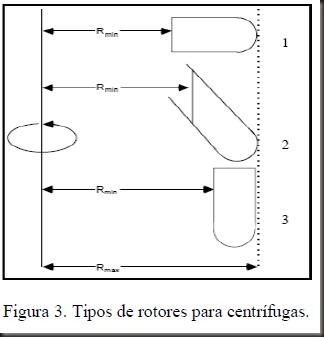
4. Tipos de rotores para centrífugas
Os rotores de centrífugas podem ser classificados como rotores móveis (1), de ângulo fixo (2) e vertical (3), sendo que cada tipo tem potências e limitações de acordo com o tipo de separação (Figura 3).
Os rotores verticais são adequados para separações isopícnicas (de densidade), como por exemplo para isolamento de DNA, RNA e lipoproteínas. Utilizam-se tubos graduados e é bastante utilizado para a determinação de volume de sedimentos. A principal desvantagem deste tipo de rotor é a ocorrência de sedimentação incompleta, pois a partícula tem que atravessar toda a “coluna” de líquido para chegar ao fundo do tubo. Para corrigir eventuais erros, utiliza-se uma rotação maior.
Em rotores de ângulo fixo, os tubos são posicionados em um ângulo definido. Ao iniciar a operação, o material se reorienta no interior do tubo, conforme a força centrífuga que é aplicada. Mais eficiente do que a centrifugação vertical, pois o caminho percorrido pela partícula é menor, é bastante utilizada em laboratórios de biotecnologia para separação de bactérias e leveduras. Este tipo de centrifugação em geral utiliza menor tempo e é eficiente para a separação de sólidos floculentos ou finamente divididos. Como principal desvantagem em relação à centrifugação vertical é não conseguir realizar a análise de volume de sedimento.
Os tubos de amostra quando inseridos em rotores móveis (1) são mantidos na vertical enquanto o equipamento está em repouso. Ao girar, se posiciona horizontalmente, dependendo da rotação que é aplicada.
Fatores para seleção de material de tubos para centrífuga: em escala laboratorial, os tubos devem ser transparentes, resistentes a solventes químicos e com boa vedação, compatibilidade química e boa recuperação da amostra.
Todo material fluido tende a expansão, gerando uma pressão sobre os tubos. Esta força (P) será somada à força centrífuga e, a somatória pode romper tubos. Atualmente, máquinas modernas possuem sistemas de proteção.
4. Tipos de Centrífuga.
 (a) Centrífuga tubular. Esta centrífuga opera geralmente na vertical, com o roto
(a) Centrífuga tubular. Esta centrífuga opera geralmente na vertical, com o roto
r tubular provendo um longo caminho para a separação da mistura. Trabalha com a força centrífuga variando de 13.000 a 20.000 g. A quantidade de sólidos na mistura limita o uso desta centrífuga, assim como a formação de bolhas que também dificulta a centrifugação.
O material a ser centrifugado é alimentado pela parte inferior, e passa por toda a tubulação para ser separado ou clarificado. A parte sólida vai depositando-se nas laterais, sendo retirada ao final do processo, enquanto os líquidos são retirados pela parte superior.
Na indústria de alimentos é utilizada para a separação e clarificação de extratos animais
e vegetais e óleo de peixe. Na indústria farmacêutica é amplamente utilizada para a
recuperação de bactérias e frações de células.
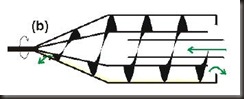
(b) Centrífuga de múltiplos discos. A câmara possui uma série de discos paralelos que
proporcionam uma grande área de sedimentação. O material é removido através de válvulas.
Em casos de clarificação de material biológico, pode-se trabalhar com a força centrífuga
variando de 5.000 a 15.000g, sendo o fluxo contínuo de alimentação de 200 m3/h.
O tamanho da partícula pode auxiliar a centrifugação. Para aumentar o tamanho da
partícula, utiliza-se o fenômeno de coagulação ou floculação. Para coagulação, realiza-se a mudança de pH da suspensão, removendo as cargas eletrostáticas da partícula e então elas aproximam-se umas às outras. Para floculação, adicionam-se pequenas quantidades de materiais de alto peso molecular, carregadas com carga oposta ao do material, promovendo agregação dos componentes que podem estes baratos e efetivos, porém, sem afetar o produto de interesse. Para favorecer a coagulação são adicionados sais de alumínio, cálcio e ferro, além de polieletrólitos sintéticos que reduzem a repulsão entre as partículas e formam pontes entre elas.
(c) Centrífuga contínua opera horizontalmente A hélice roda e distribui os sólidos ao
longo da superfície do recipiente, retirando-o do líquido. O liquido sai pelo outro lado da câmara. O parafuso roda em velocidade diferente da câmara
(d) Centrífuga de Cestos
A centrífuga de cestos pode ser classificada como perfurada e não perfurada. A centrífuga perfurada associa as operações de centrifugação e filtração em conjunto, assemelhando-se ao tambor de uma máquina de lavar, por exemplo. Então, neste caso
especifico, pode-se considerar a centrifugação como uma operação de pré-secagem. No caso de sólidos cristalinos, utiliza-se o cesto sem filtros e no caso de partículas deformáveis, como por exemplo, proteínas.
No caso de cestos não perfurados, a ação é apenas da força centrífuga. As partículas sólidas tendem a se acumular nas paredes da centrífuga e, com o passar do tempo estas começam a ser liberadas junto com o filtrado.
Outras características também devem ser consideradas como, por exemplo, o uso de refrigeração no caso de tratamento de material biológico, centrífugas providas de aquecimento que alteram a viscosidade e a solubilidade do material.
5. Tipos de separação centrífuga.
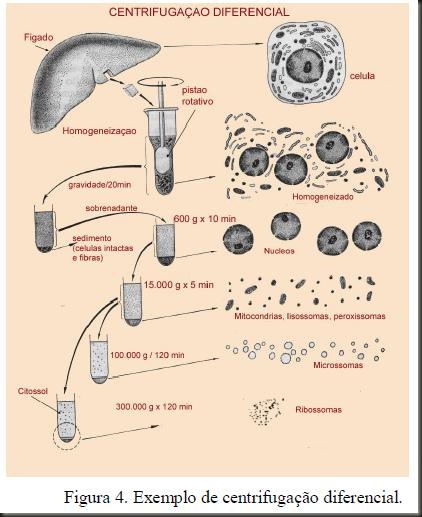
A) Centrifugação diferencial
A separação é baseada no tamanho das partículas. Uma suspensão contendo diferentes moléculas é centrifugada e as partículas maiores sedimentam com mais rapidez do que as partículas menores, obtendo-se frações de moléculas.
Exemplo: quando uma suspensão de material biológico é deixado em repouso, as células intactas se depositam. Se centrifugados a 600g por 10 minutos, os núcleos densos sedimentam para o fundo do tubo. O sobrenadante é então centrifugado a 15.000g por 5 minutos para separar mitocôndrias e assim sucessivamente. Algumas destas organelas em sedimentação podem ser obtidas em pureza parcial, e em geral elas estão contaminadas com outras partículas, servindo como etapa preliminar para posterior purificação usando outros tipos de separação centrífuga.
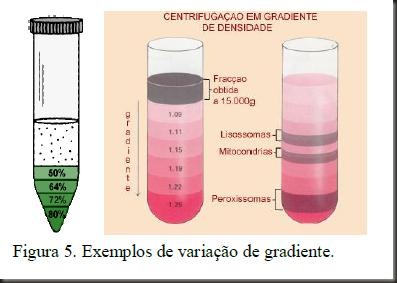
B. Centrifugação por gradiente
A centrifugação diferencial não permite separar diferentes moléculas que se depositem em uma mesma etapa de centrifugação, embora possuam densidades diferentes. Para tanto, faz-se uso da centrifugação por gradiente, submetendo a suspensão de partículas a uma força centrífuga constante, em meio de densidade /peso gradualmente variável, de uma extremidade à outra do tubo. A fração celular a ser separada é colocada sobre a camada e centrifugada. Empregam-se substâncias como a sacarose. As partículas com densidades diferentes, se deslocam até alcançar o local de igual densidade. A separação por gradiente pode ser classificada em duas categorias: por índice regional (tamanho) e Separação isopícnica (densidade).
As frações isoladas podem, posteriormente, ser submetidas a uma gama diversificada de análises bioquímicas, para se identificar a composição química, a atividade enzimática, bem como as capacidades metabólicas.
– Separação gradiente de tamanho. Esta separação baseia-se no tamanho e massa da partícula para sedimentação. Uma utilização para este tipo de centrifugação é a separação de proteínas e anticorpos, que possuem densidades similares, porém massas diferentes. Assim, a separação com base na massa separará as diferentes classes.
Para que a centrifugação por tamanho seja bem sucedida, a densidade da solução de amostra deve ser inferior à menor densidade do gradiente; a extensão do gradiente devem ser suficiente para ocorrer a separação e o tempo deve ser bem dimensionado, pois se for muito extenso, as partículas podem ser acumular no fundo do tubo.
– Separação isopícnica. Neste caso, vamos considerar uma partícula que possui uma determinada densidade e, que será submetida ao processo de centrifugação. Após o processo, a partícula irá “estacionar” em uma posição onde a densidade da solução em que se encontra é próxima à densidade da partícula. Uma vez estabelecida a sua posição, o tempo total de centrifugação não irá alterar a migração da partícula. Uma aplicação bastante utilizada para este método é a separação de ácidos nucléicos em um gradiente de cloreto de césio (CsCl).
Para que a centrifugação seja bem sucedida, a densidade da partícula da amostra deve estar dentro dos limites das densidades de gradiente; qualquer extensão de gradiente é aceitáv
el; o tempo de execução deve ser suficiente para que as partículas se unam em seu ponto isopícnico.
C. Ultracentrifugação
Processo de centrifugação sob pressão, permitindo a separação de partículas de modo eficiente, utilizando-se de refrigeração e vácuo de forma a minimizar o atrito com o ar, devido à elevada rotação aplicada (até 500.000g).
6. Conversão de unidades de centrifugação.
A rotação de uma centrífuga pode ser especificada em termos de Força Centrífuga Relativa (RCF) expressa em unidades de gravidade (g). Muitas centrífugas expressam a velocidade em termos de revoluções por minuto (rpm).
A conversão entre g (a força centrífuga) e rpm é dada pela relação:
onde: Fc = força centrífuga;
FCR = força centrífuga relativa;
R = diâmetro do rotor (cm)
S = velocidade da centrífuga (rpm)
M = massa da amostra
No caso do cálculo da Força centrífuga relativa, esta não considera a massa da amostra, ou a sua densidade. Quando se troca a centrífuga, deve-se recalcular o g.
7. Aplicações da centrifugação
A centrifugação pode ser utilizada além de apenas uma operação unitária na indústria. É também bastante aplicada em casos de tratamentos de fertilidade e, existem estudos que avaliam a possibilidade de separação de espermatozóides que não contenham o vírus da AIDS, para a geração de uma criança não portadora do vírus. Esta seleção realizada para humanos é utilizada em gado, com o objetivo de criar as melhores cabeças de gado, rebanho, tornando o negócio mais lucrativo.
Além da inseminação, a centrifugação, é utilizada no processo de enriquecimento de urânio. A NASA também utiliza uma espécie de centrífuga onde seus astronautas são submetidos a forças de até 20 g.
8. Referências
PESSOA JR, A. KILIKIAN, B. V., Purificação de Produtos Biotecnológicos , p. 30 a 36, Editora Manole, 2005.
http://www.lsbu.ac.uk/biology/enztech/centrifugation.html
REVISTA VEJA, 22 de setembro de 2004.
Cole-Parmer site, http://www.coleparmer.com/techinfo/techinfo.asp?htmlfile= basic-centrifugation.htm&ID=30